Механизм действия и функции
Аспарагиновая кислота – альфа-аминокислота с химической формулой HOOCCH (NH2) CH2COOH.
Современные биологические исследования подтвердили ее способность влиять на работу эндокринной системы. DAA стимулирует выработку гонадотропина, который помогает синтезу тестостерона – главного анаболика у спортсменов, работающих с тяжелым весом.
Западные бодибилдеры и пауэрлифтеры активно используют аспартат для повышения эффективности тренировок: увеличения показателей силы, выносливости и объемов мышц. В России БАДы только начинают набирать популярность. Принимая эту кислоту, можно получить:
- усиленную выработку тестостерона;
- повышение количества гонадотропина;
- быстрый рост мышц;
- увеличение силовых показателей и быстрое восстановление после тренировок.
Содержание в продуктах
Организм способен самостоятельно вырабатывать аспарагин в оптимальном для обычного человека количестве. Получить его можно из пищи, особенно важны высокобелковые продукты:
- мясо;
- рыба;
- яйца;
- авокадо;
- спаржа;
- орехи;
- пивные дрожжи;
- картофель;
- нежирные сливки;
- кукурузный протеин.
Виды и формы добавок
Еще до начала использования добавок с D-аспарагиновой кислотой препараты на ее основе выпускались в Италии – в качестве лекарства от бесплодия под наименованием DADAVIT.
Добавки с кислотой имеют обозначение D-Aspartic Acid. Популярны следующие БАДы:
- Порошки: DAA D-Aspartic Ac >Спортсмены отмечают, что наиболее удобными формами являются капсулы и таблетки – порошок не очень приятен на вкус и плохо растворяется. Если БАД приобретен в виде последнего, его лучше превратить в суспензию – развести в 50 мл сока, а после приема запивать водой.
Сочетаемость с другими веществами
Существуют доказательства того, что чувствительность к DAA зависит от возраста, состояния эндокринной системы, режима тренировок и диеты спортсмена. В спортивном питании аминокислоту можно сочетать с протеиновыми коктейлями, гейнерами и любимыми специальными добавками, однако перерыв между приемом разных веществ должен составлять 15-20 минут.
Аспарагиновая кислота повышает уровень пролактина в крови, поэтому после курса стероидов необходимо сделать перерыв, минимизирующий их действие – только после этого можно начинать следующий курс приема DAA.
Правила приема
Максимального эффекта от воздействия вещества можно добиться, используя циклическую схему: 3 недели приема с перерывом в 2 недели. Эффективность оценивают по окончании первого цикла.
Начальная доза вещества – 3 г/сутки. Их делят на три части и принимают на пустой желудок утром, в обед и вечером. При необходимости можно увеличить дозу до 20 г/сутки.
Принимать DAA в максимально разрешенных инструкцией дозах нужно лишь в отдельных случаях – большинство спортсменов получают положительный результат от приема 5-10 г/сутки. Курс длительностью менее 3 недель подряд будет не очень результативным, а продление курса приводит к снижению эффективности действия кислоты – выработка тестостерона при длительном приеме резко снижается.
Противопоказания и побочные эффекты
Прямые показания к приему аминокислоты:
- низкое либидо;
- медленное восстановление после тренировок;
- низкий уровень тестостерона;
- снижение эндогенного синтеза анаболических гормонов.
После отмены препарата организм продолжает синтез тестостерона в естественном режиме. Несмотря на это, прием аспарагиновой кислоты противопоказан:
- женщинам, поскольку воздействие кислоты на их организм еще не изучено;
- мужчинам до 21 года;
- при повышенной выработке тестостерона, дигидростерона, эстрогена;
- при нарушениях работы гормональной системы;
- лицам, страдающим заболеваниями печени, почек, сахарным диабетом.
Прием кислоты может привести к некоторым побочным эффектам:
- Повышенный уровень дигидростерона вызывает развитие акне и выпадение волос.
- Усиленная выработка эстрогенов может привести к гинекомастии, метеоризму, воспалению простаты и снижению либидо.
- Рост андрогенов в крови, что вызывает повышение агрессии.
Передозировка аминокислоты (более 20 г/сутки) может вызвать сильные головные боли, депрессию, расстройство работы ЖКТ, падение артериального давления и сгущение крови.
D-аспарагиновая кислота используется бодибилдерами для достижения высоких результатов в силовых тренировках. Главное условие – использовать добавку разумно и контролировать ее воздействие на организм.
Продукты богатые аспарагиновой кислотой:
Общая характеристика аспарагиновой кислоты
Аспарагиновая кислота относится к группе аминокислот, обладающих эндогенными свойствами.
Это означает, что помимо ее присутствия в продуктах питания, она также может образовываться в самом организме человека.
Физиологами был выявлен интересный факт: аспарагиновая кислота в организме человека может присутствовать как в свободном виде,
так и в виде белковых соединений.
В нашем организме аспарагиновая кислота выполняет роль медиатора, который отвечает за правильную передачу сигнала от одного нейрона к другому.
Кроме того, кислота славится своими нейропротекторными свойствами. Во время стадии эмбрионального развития,
в организме будущего человека наблюдается повышение концентрации кислоты в сетчатке и головном мозге.
Аспарагиновая кислота, помимо естественного присутствия в продуктах
питания, выпускается в форме таблеток для лечения сердечных недугов,
используется как пищевая добавка для придания напиткам и кондитерским
изделиям кисло-сладкого вкуса, а также применяется как препарат спортивного
питания в бодибилдинге. В составе ингредиентов она обычно значится
как D-Aspartic acid.
Суточная потребность в аспарагиновой кислоте
Суточная потребность в кислоте для взрослого человека – не более 3 грамм в сутки.
При этом употреблять ее следует в 2-3 приема, так рассчитав ее количество, чтобы на один прием пищи приходилось не более 1-1,5 грамма.
Потребность в аспарагиновой кислоте возрастает:
- при заболеваниях связанных с нарушением функционирования нервной системы;
- при ослаблении памяти;
- при заболеваниях головного мозга;
- при психических расстройствах;
- депрессии;
- снижении работоспособности;
- при возникновении проблем со зрением («куриная слепота», миопия);
- при заболеваниях сердечно-сосудистой системы;
- после 35-40 лет. Также ребуется проверять баланс между аспарагиновой кислотой и тестостероном (мужским половым гормоном).
Потребность в аспарагиновой кислоте снижается:
- при заболеваниях, связанных с повышенным образованием мужских половых гормонов;
- при высоком артериальном давлении;
- при атеросклеротических изменениях сосудов головного мозга.
Усваиваемость аспарагиновой кислоты
Усваивается аспарагиновая кислота очень хорошо. Однако, вследствие того, что она способна объединяться с белками,
она может вызывать привыкание. В результате этого, пища без данной кислоты будет казаться безвкусной.
Полезные свойства аспарагиновой кислоты и ее влияние на организм:
- укрепляет организм и повышает работоспособность;
- участвует в синтезе иммуноглобулинов;
- играет важнейшую роль в обмене веществ;
- ускоряет восстановление при усталости;
- помогает извлекать энергию из сложных углеводов для формирования ДНК и РНК;
- способна деактивировать аммиак;
- помогает печени выводить из организма остаточные элементы химикатов и лекарств;
- помогает ионам калия и магния проникать внутрь клетки.
Признаки нехватки аспарагиновой кислоты в организме:
- ухудшение памяти;
- депрессивное настроение;
- снижение работоспособности.
Признаки избытка аспарагиновой кислоты в организме:
- перевозбуждение нервной системы;
- повышенная агрессивность;
- сгущение крови.
Безопасность
Врачи не рекомендуют регулярно употреблять продукты, содержащие аспарагиновую кислоту в ненатуральном виде.
Особенно это касается детей, чья нервная система чрезвычайно чувствительна к данному веществу.
У детей данная кислота может вызвать привыкание, в результате чего
они могут полностью отказаться от продуктов, не содержащих аспарагинаты.
Для беременных, употребление большого количества продуктов, содержащих
аспарагиновую кислоту, может негативно сказаться на нервной системе
ребенка, вызвав аутизм.
Наиболее приемлемой для человеческого организма является кислота, изначально присутствующая в продуктах питания в естественном виде.
Природная аспарагиновая кислота не вызывает привыкания организма.
Что же касается использования D-Aspartic acid в качестве
усилителя вкуса, то данная практика нежелательна, в связи с возможностью
возникновения пищевого пристрастия, на фоне которого продукты без
данной добавки будут казаться безвкусными и совсем не привлекательными.
Внимание! Информация носит ознакомительный характер и не предназначена для постановки диагноза и назначения лечения. Всегда консультируйтесь с профильным врачом!. Полезность материала
10
Достоверность информации
Оформление статьи
Полезность материала
10
Достоверность информации
Оформление статьи
Аспарагиновая кислота: применение
Аспарагиновая кислота применяет в нескольких, совершенно разных случаях, таких как:
- депрессивное состояние (избавиться также можно с помощью рыбьего жира, адеметионина, фосфатидилсерина);
- когнитивные расстройства (нарушение мышления, ухудшение памяти);
- эректильная дисфункция и снижение сексуальной активности;
- с целью наращивания мышц для спортсменов;
- гормональный дисбаланс (дефицит гормонов);
- расстройства ЦНС;
- для терапии сердечнососудистых заболеваний;
- нарушение зрения (близорукость, никталопия);
- токсичное загрязнение печени;
- синдром хронической усталости;
- послеоперационный период или восстановление после тяжелой болезни.
Важно, что при недостаточном количестве аминокислоты в организме у пациентов наблюдается ухудшение памяти, подавленное состояние и нежелание заниматься активной деятельностью. Однако при повышенном количестве вещества в организме человек чувствует себя нервным и агрессивным, неспособен контролировать эмоции
Даже наблюдаются изменения в густоте крови, что нередко становится причиной тромбов в кровеносных сосудах.
Обычно применение аспарагиновой кислоты необходимо для всех людей после 40 лет. В этом возрасте даже у здорового человека начинает снижаться ее уровень. Поэтому, чтобы предупредить возможные заболевания, кислоту желательно принимать и без веской на то причины.
Добавки аспарагина
В обычном режиме и при сбалансированном питании образование аспарагина в нашем организме полностью обеспечивает все потребности и мы не испытываем нехватки этого вещества. Но при напряженных тренировках, интенсивной работе, некоторых заболеваниях нервной системы, сердца, глаз, потребность в этом веществе резко возрастает.
Много аспарагина содержится в говядине и курином мясе, морской рыбе и морепродуктах, яйцах и молочной сыворотке. Из растительной пищи богаты аминокислотой спаржа, пшеница, соя, арахис, цитрусовые, картофель, помидоры.
Но в некоторых случаях могут оказаться полезны добавки с аспарагином. Необходимо только следить за соблюдением дозировок.
Суточная норма употребления аспарагина по разным исследованиям составляет 3 -6 грамм. При повышенном артериальном давлении, атеросклерозе суточную норму необходимо снижать. О переизбытке в организме аминокислоты аспарагина может говорить нарушение сна, повышенная возбудимость, раздражительность, головные боли. Сгущение крови также должно стать сигналом для уменьшения дозировки препаратов аспарагина. Чтобы избежать этого, дополнительный прием аспарагина следует обязательно согласовать с врачом.
Общая характеристика
Натуральная аспарагиновая кислота с формулой C4H7NO4 представляет собой бесцветные кристаллы с высокой температурой плавления. Другое название вещества – аминоянтарная кислота.
Все аминокислоты, используемые человеком для синтеза белка (кроме глицина), имеют по 2 формы. И только L-форма применяется для синтеза белка и роста мышц. D-форма также может использоваться человеком, но при этом выполняет несколько другие функции.
- Общая характеристика
- Различия между формами
- Роль L-изомера
- Польза D-изомера
- Суточные нормы
- Кому нужны повышенные дозы
- Аминокислотный дефицит
- Пищевые источники
Аспарагиновая аминокислота также существует в 2 конфигурациях. L-аспарагиновая кислота более распространенная и принимает участие во многих биохимических процессах. Биологическая роль D-формы не столь разнообразна, как ее зеркального изомера. Организм в результате ферментативной деятельности способен происходить обе формы вещества, которые затем образуют так называемую рацемическую смесь DL-аспарагиновой кислоты.
Наивысшая концентрация вещества найдена в клетках головного мозга. Воздействуя на центральную нервную систему, повышает концентрацию и способности к обучению. Исследователи говорят, что повышенная концентрация аминокислоты содержится в мозге людей, страдающих эпилепсией, а вот у лиц с депрессиями, наоборот, значительно меньше.
Аспарагиновая кислота, вступая в реакцию с другой аминокислотой – фенилаланином, образует аспартам. Этот искусственный подсластитель активно применяется в пищевой промышленности, а на клетки нервной системы действует как раздражитель. По этой причине врачи не рекомендуют к частому использованию добавки на основе аспарагиновой кислоты, особенно детям, чья нервная система более чувствительна. У них на фоне аспарагинатов возможно развитие аутизма. Также аминокислота может влиять на женское здоровье и регулировать химический состав фолликулярной жидкости, что уменьшает репродуктивный потенциал. А частое потребление аспарагинатов беременными может негативно сказаться на здоровье плода.
Роль в организме:
- Аспарагиновая кислота важна в процессе формирования других аминокислот, таких как аспарагин, метионин, изолейцин, аргинин, треонин и лизин.
- Избавляет от хронической усталости.
- Важна для транспортировки минералов, необходимых для формирования и функционирования ДНК и РНК.
- Укрепляет иммунную систему, способствуя выработке антител и иммуноглобулинов.
- Положительно влияет на работу центральной нервной системы, поддерживает концентрацию внимания, обостряет работу мозга.
- Способствуют выведению токсинов из организма, в том числе аммиака, который крайне негативно сказывается на работе мозга, нервной системы и печени.
- В условиях стресса организм нуждается в дополнительных дозах аминокислоты.
- Является эффективным средством против депрессий.
- Способствует преобразованию углеводов в энергию.
Какие аминокислоты в клетках человека называются незаменимыми?
Начинать изучать незаменимые для человека аминокислоты следует с такого вещества как аргинин: укрепляет иммунитет. Он регулирует уровень окиси азота, ответственной за управление кровотоком, иммунитетом, коммуникацией между нервными клетками, функцией печени, свертыванием крови и даже половым возбуждением. В организме человека незаменимые аминокислоты подобного типа не синтезируются в принципе и их дефицит может привести к необратимым последствиям.
Окись азота (N0) — «фактор расслабления», так как при ее действии расслабляются кровеносные сосуды, и снижается артериальное давление. Но самостоятельно принимать аргинин нельзя: избыток окиси азота, выделяемый из аргинина, как и ее недостаток, опасны для здоровья. Когда будут разработаны точные способы определения содержания окиси азота в сыворотке крови, тогда будет ясно, нуждается ли организм в его дополнительном количестве, и будет назначен аргинин, но вместе с другими антиоксидантами.
Аргинин сам по себе, а не окись азота, которая образуется из него, снижает уровень холестерина эффективнее других аминокислот.
Окись азота, расслабляя стенки артерий, способствует свободному протеканию крови, применяется при заболевании сосудов сердца и конечностей. Но роль аргинина заключается не только в выработке окиси азота, он участвует в формировании мышц и других безжировых тканей организма. Еще аргинин — сырье для синтеза орнитина, другой аминокислоты в клетках человека, отвечающей за уровень защиты от вторжения болезнетворных агентов.
Выбор того, какие аминокислоты и дозы использовать, зависит от цели, одновременно нужно принимать кофермент Q10 и липоевую кислоту. До 18 лет не применяются ни большие дозы, ни длительный прием, так как это способствует активному выделению гормона роста, что может стать неблагоприятным фактором для растущего организма.
Рекомендуется предварительно проконсультироваться с врачом относительно того, какие аминокислоты незаменимые для укрепления иммунитета принимается вместе с лизином.
Кофермент Q10 (убихинон) играет важную роль в процессе выработки энергии в каждой клетке организма, увеличивает продолжительность жизни клеток. Сам термин означаем «вездесущий»: он есть в каждой клетке организма. Но выработку энергии — не единственная функция кофермента Q10, он защищает организм от свободных радикалов и усиливает иммунитет. Поэтому обязательно входит в программу профилактики и лечения сердечно-сосудистых заболеваний, диабета, гипертонии, ожирения, рака. Главное — убихинон замедляет процесс старения!
Учеными давно изучено, какие аминокислоты называются незаменимыми, однако для восполнения их дефицита далеко не всегда достаточно употреблять в пищу полный рацион, рекомендованный диетологами. В продуктах питания содержатся лишь следы кофермента Q10, для оптимального количества в организме нужен его дополнительный прием. Сердце расходует очень много энергии. Его работа зависит от наличия кофермента, при дефиците которого в 75 % сердце останавливается.
Когда кофермент принимали больные, нуждающиеся в пересадке сердца, их состояние значительно улучшалось. Он помогает при кардиомиопатии, аритмии и других заболеваниях сердца. Главное достоинство — отсутствие побочных эффектов. У больных с сердечной недостаточностью улучшается функция легких, уменьшается отечность. В отличие от лекарств, кофермент эффективно воздействует на факторы, вызывающие атеросклероз.
Применяется при избытке веса. Потеря веса происходит, потому что кофермент использует жировые запасы в качестве источника энергии.
Кофермент Q10 активизирует иммунную систему. А это свойство используется в борьбе с онкологическими процессами. Он снижет артериальное давление и уровень сахара крови. Были проведены исследования, сообщающие об эффективности кофермента Q10 при параличе лицевого нерва и других заболеваниях. Но лучшее, что может дать кофермент, — это борьба с усталостью. Пик его выработки — в 20 лет, к 80 годам выработка этого вещества снижается на 60 %.
Пищевыми источниками являются мясные субпродукты (сердце, почки и др.), красное мясо, орехи, нерафинированное масло.
Липоевая кислота — проверенное средство при диабете. Несколько лет назад о ней никто и не слышал, а сейчас это признанный антиоксидант и главное средство для лечения диабетической нейропатии. Действуя как антиоксидант, она и сама служит защитой таких антиоксидантов, как глутатион, витамины С и Е, кофермент Q10- Таких свойств нет ни у одного вита-нутриента. Кислота предотвращает отложение жира и выводит токсины и другие продукты метаболизма жира. Причиной повреждения нервов при диабете является избыток сахара в крови.
Доступность
D-аспарагиновая кислота (D-AA) является аминокислотным регулятором синтеза тестостерона и может оказывать влияние на стимулирующий рецептор (рецептор N-метил-D-аспартата). D-AA может оказывать позитивное влияние на мужскую фертильность. Выпускается в виде аминокислотной добавки.
:Tags
Читать еще: Беназеприл (беназеприла гидрохлорид) , Ланреотид , Мепакт (Мифамуртид) , Муира пуама , Транексамовая кислота ,
Список использованной литературы:
Dietary D-amino acids
Friedman M. Chemistry, nutrition, and microbiology of D-amino acids. J Agric Food Chem. (1999)
Perna AF, et al. D-aspartate content of erythrocyte membrane proteins is decreased in uremia: implications for the repair of damaged proteins. J Am Soc Nephrol. (1997)
Wolosker H, D'Aniello A, Snyder SH. D-aspartate disposition in neuronal and endocrine tissues: ontogeny, biosynthesis and release. Neuroscience. (2000)
Topo E, et al. The role and molecular mechanism of D-aspartic acid in the release and synthesis of LH and testosterone in humans and rats. Reprod Biol Endocrinol. (2009)
d-amino acid oxidase II. Specificity, competitive inhibition and reaction sequence
Raucci F, D'Aniello S, Di Fiore MM. Endocrine roles of D-aspartic acid in the testis of lizard Podarcis s. sicula. J Endocrinol. (2005)
Davies LP, Johnston GA. Uptake and release of D- and L-aspartate by rat brain slices. J Neurochem. (1976)
Erreger K, et al. Subunit-specific agonist activity at NR2A-, NR2B-, NR2C-, and NR2D-containing N-methyl-D-aspartate glutamate receptors. Mol Pharmacol. (2007)
Topo E, et al. Evidence for the involvement of D-aspartic acid in learning and memory of rat. Amino Acids. (2010)
Aspartate racemase, generating neuronal D-aspartate, regulates adult neurogenesis
d-Aspartic acid supplementation combined with 28 days of heavy resistance training has no effect on body composition, muscle strength, and serum hormones associated with the hypothalamo-pituitary-gonadal axis in resistance-trained men
Expression of metabotropic glutamate receptors in the rat and human testis
Nagata Y, et al. Stimulation of steroidogenic acute regulatory protein (StAR) gene expression by D-aspartate in rat Leydig cells. FEBS Lett. (1999)
Chandrashekar KN, Muralidhara. D-Aspartic acid induced oxidative stress and mitochondrial dysfunctions in testis of prepubertal rats. Amino Acids. (2010)
D-Aspartate, a Key Element for the Improvement of Sperm Quality
D'Aniello G, et al. Reproductive implication of D-aspartic acid in human pre-ovulatory follicular fluid. Hum Reprod. (2007)
Hsu C, et al. Blockage of N-methyl-D-aspartate receptors decreases testosterone levels and enhances postnatal neuronal apoptosis in the preoptic area of male rats. Neuroendocrinology. (2000)
Long Z, et al. d-Aspartate in a prolactin-secreting clonal strain of rat pituitary tumor cells (GH(3)). Biochem Biophys Res Commun. (2000)
D'Aniello G, et al. The role of D-aspartic acid and N-methyl-D-aspartic acid in the regulation of prolactin release. Endocrinology. (2000)
Ishio S, et al. D-aspartate modulates melatonin synthesis in rat pinealocytes. Neurosci Lett. (1998)
Yamada H, et al. Functional expression of a GLT-1 type Na+-dependent glutamate transporter in rat pinealocytes. J Neurochem. (1997)
D-Aspartate, a Key Element for the Improvement of Sperm Quality
Errico F, et al. A physiological mechanism to regulate D-aspartic acid and NMDA levels in mammals revealed by D-aspartate oxidase deficient mice. Gene. (2006)
Функции аспарагиновой кислоты: переаминирование
Аминный азот практически всех аминокислот (за исключением лизина, треонина и пролина) через посредство ферментов аминотрансфераз переходит на глутамат. Аминный азот этих трех аминокислот тоже в конечном итоге оказывается в составе глутаминовой кислоты, но более сложным путем. Так осуществляется депонирование аминного азота в организме. Накопление аминного азота в форме глутаминовой кислоты происходит в цитозоле клеток. Затем специфические ферменты транслоказы переносят глутамат в митохондрии, где активна специфическая АСТ. АСТ превращает глутамат опять в α-кетоглутарат, а тот вновь вступает в реакции переаминирования, принимая на себя аминные головы различных аминокислот, и вновь превращаясь в глутамат.
Аспартат (аспарагиновая кислота), образующийся в митохондриях в реакциях транс аминирования между оксалацетатом и глутаматом, может транспортироваться в цитозоль клетки, где он отдает аминную группу NH3 в цикл мочевины, образуя аминокислоту аргинин. Это реакция, составляющая Аспартат-АргининоСукцинатный шунт, обеспечивают связь между путями, в которых утилизируется аминогруппы и углеродный скелет аминокислот. Утилизация аминогрупп в синтезе безвредной мочевины происходит в клетках печени, и в меньшей степени почек.
Реакции трансаминирования являются начальным этапом распада аминокислот в организме. В результате аминный азот через аспарагиновую кислоту перебрасывается на глутаминовую кислоту, а углеродный скелет либо сгорает в цикле Кребса с образованием энергии, либо идет на синтез глюкозы и кетоновых тел. Аспарагиновая кислота выступает посредником в передаче аминного азота в депо, каковым выступает глутаминовая кислота. Только глутаминовая кислота в тканях человека способна подвергаться прямому окислительному дезаминированию. Все остальные аминокислоты подвергаются непрямому дезаминированию с перебросом аминных групп NH3 первоначально на глутаминовую кислоту, а вторым этапом происходит дезаминирование глутамата.
В мышечной ткани при интенсивной физической нагрузке функционирует другой путь непрямого дезаминирования с непосредственным участием аспарагиновой кислоты. Начальный путь такой же, как и при обычном непрямом дезаминировании, когда аминные группы почти всех аминокислот собираются на глутамат. Потом с глутамата они перебрасываются на аспартат (аспарагиновую кислоту), затем аминная голова с аспартата перекидывается на инозиновую кислоту (ИМФ), в результате получается АМФ. Аспартат, лишившись аминной головы, превращается в фумарат. Далее фумарат по цепочке Цикла Кребса превращается в малат, а тот в оксалацетат, который ловит аминную голову с глутамата, чтобы превратиться в аспартат. Так обеспечивается работа конвейера по переброске аминного азота со всего пула аминокислот на ИМФ. АМФ подвергается гидролитическому дезаминированию, т.е фермент АМФ-дезаминаза откусывает аминную голову у АМФ, получается ИМФ, которая опять готова к работе на конвейере и свободный аммиак NH3.
Представленная схема отражает последовательность реакций непрямого окислительного дезаминирования в мышечной ткани при интенсивной физической нагрузке.
При интенсивной мышечной работе, когда задействован данный путь дезаминирования, одновременно утилизируется глюкоза с образованием молочной кислоты (лактата), что приводит к закислению внутренней среды клетки, а это нежелательно. Выделяющийся аммиак имеет щелочную реакцию и нейтрализует избыточную кислотность.
Можно выделить 4 стадии процесса:
- Трансаминирование с α-кетоглутаратом, образование глутамата
- Трансаминирование глутамата с оксалацетатом (фермент АСТ), образование аспартата
- Реакция переноса аминогруппы с аспаратата на инозиновую кислоту (ИМФ, ИнозинМоноФосфат), образование АМФ (АденозинМоноФосфат) и фумарата
- Гидролитическое дезаминирование АМФ с выделением аммиака NH3.
Химические реакции первых двух стадий были представлены выше.
Третьей стадией является реакция переноса аминогруппы с аспартата на инозиновую кислоту происходит в два этапа. На первом этапе под воздействием фермента АденилоСукцитанСинтетазы Аспарагиновая кислота присоединяется к ИМФ, в результате образуется АденилоСукцинат. Процесс идет с затратой энергии, которую отдает ГТФ (ГуанозинТри Фосфат), при этом отщепляется остаток фосфорной кислоты, а ГТФ превращается в ГДФ (ГуанозинДиФосфат). Затем фермент АденилоСукцинат Лиаза расщепляет АденилоСукцинат на АМФ (АденозинМоноФосфат) и Фумаровую кислоту (Фумарат).
Аспарагиновая кислота: синтез, образование
Процесс синтеза аспарагиновой кислоты живым организмом происходит путем превращения незаменимой аминокислоты треонин в изомер другой аминокислоты – гомосерина с дальнейшими окислительными реакциями.
Впервые вещество было обнаружено в начале 19 века. Ученые Этьен Оссиана Генри и Огюст-Артур Плиссон получили кислоту в результате реакции взаимодействия вещества аспарагина с водой в присутствии сильных минеральных кислот. Предварительно аспарагин был выделен из сока спаржи путем кипения. Спустя несколько лет аспарагиновая кислота была признана важнейшей составляющей белков.
В современном производстве аминокислоту получают с помощью конденсации нескольких эфиров (ацетаминомалонового и хлоруксусной кислоты). Из полученных продуктов отщепляют карбоксильную группу с последующим гидролизом.
Чтобы восполнить недостаток аспарагиновой кислоты в организме, можно употреблять некоторые продукты: мясо, тростник, спаржа, овсяные хлопья, авокадо, соевые бобы. В этой пище аминокислота содержится в слишком маленьком количестве, поэтому для лекарственных целей подходят только БАДы с высокой концентрацией вещества.
Синтез аспарагиновой кислоты и фермент АСТ
Синтез аспарагиновой кислоты непрерывно идет в организме. Еще бы, ведь она вместе с глутаминовой кислотой является этаким складом аминных групп NH2. Аминокислоты превращаются друг в друга в реакциях переаминирования. При поступлении аминокислот в организм, ферменты трасферазы рубят аминные головы и насаживают их — нет, не на колья — а синтезируя глутамат и аспарагинат. Активным участником реакции переаминирования является пиридоксальфосфат или витамин В6. Он заставляет работать фермент трансферазу, принимая на себя аминную голову от глутамата и передавая ее оксалацетату, который превращается в аспарагиновую кислоту. Оксалацетат — продукт превращения глюкозы в Цикле Кребса, он сам может превратиться в глюкозу, а может стать источником аспарагиновой кислоты.
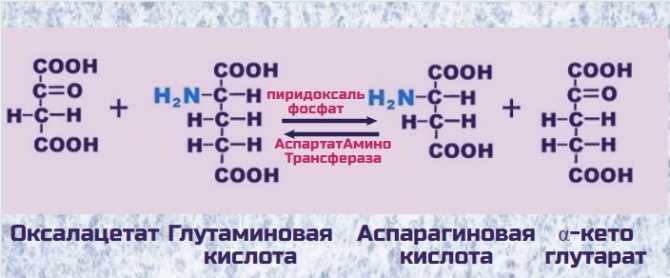
Фермент АспартатАминоТрансфераза, иначе говоря АСТ (АсАТ) имеет как цитоплазматическую, так и митохондриальную формы. В наибольшем количестве он содержится в клетках сердечной мышцы (миокарде) и печени (гепатоцитах), в значительных количествах он имеется в скелетной мускулатуре. Содержание его в крови очень низкое, т.е. данный фермент является органоспецифичным. Заметно, что максимальный уровень фермента имеется в сократительных клетках, которые выполняют механическую работу (кардиоциты, миоциты), т.е. там, где выделяется много аминного азота. Клетки печени также выполняют специфическую работу по утилизации лишнего аминного азота, синтезируя из вредного аммиака безвредную мочевину. Для всех этих целей требуется аспарагиновая кислота.
При разрушении клеток сердца, печени или скелетной мускулатуры при заболевании (инфаркт миокарда, гепатит, травмы) фермент АСТ поступает в кровь, и его содержание значительно увеличивается. Увеличение АСТ имеет диагностическое значение и свидетельствует о процессе, сопровождающемся разрушением клеток внутренних органов, в первую очередь сердечной мышцы, печени, поджелудочной железы, скелетной мускулатуры при обширных травмах.
Ссылки [ править ]
- ^ Будавари, Сьюзен; Ко, Мерк (1989). . (11-е изд.). п. . ISBN
- . inchem.org .
- Хейнс, Уильям М., изд. (2016). CRC Справочник по химии и физике (97-е изд.). CRC Press . С. 5–89. ISBN 978-1498754286.
- . Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано из 9 октября 2008 года . Проверено 5 марта 2018 .
- ^ Г., Воет, Джудит; В., Пратт, Шарлотта (29 февраля 2016 г.). Основы биохимии: жизнь на молекулярном уровне . ISBN . OCLC .
- Берцелиус JJ , Öngren OG (1839). (на французском). 3 . Брюссель: A. Wahlen et Cie. P. 81 . Проверено 25 августа 2015 года .
- Плиммер R (1912) . Плиммер Р., Хопкинс Ф. (ред.). . Монографии по биохимии. Часть I. Анализ (2-е изд.). Лондон: Longmans, Green and Co., стр. 112 . Проверено 18 января 2010 года .
- «Номенклатура и символика аминокислот и пептидов (Рекомендации IUPAC-IUB 1983)», Pure Appl. Chem. , 56 (5): 595-624, 1984, DOI.
- Карлхайнц Drauz, Ян Грейсон, Axel Kleemann, Ханс-Петер Криммер, Вольфганг Leuchtenberger, Кристоф Weckbecker (2006). Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI .
- ↑ Dunn MS, Smart BW (1950). . Органический синтез . 30 : 7.; Сборник , 4 , с. 55.
- Ленинджер AL, Нельсон Д.Л., Кокс М. (2000). Принципы биохимии (3-е изд.). Нью-Йорк: У. Х. Фриман. ISBN 1-57259-153-6.
- Kreamer, Siegel, и Горли (октябрь 2001). . Педиатрические исследования . 50 (4): 460–466. DOI . PMID .
- Chen PE, Geballe MT, Stansfeld PJ, Johnston AR, Yuan H, Jacob AL, Snyder JP, Traynelis SF, Wyllie DJ (май 2005 г.). «Структурные особенности сайта связывания глутамата в рекомбинантных N-метил-D-аспартатных рецепторах NR1 / NR2A, определенные с помощью сайт-направленного мутагенеза и молекулярного моделирования». Молекулярная фармакология . 67 (5): 1470–84. DOI . PMID . S2CID .
- . Grand View Research . Проверено 30 ноября 2019 года .
- ↑ Evans J (2014). . BCC Research. С. 101–103.
- ^ Исследование рынка прозрачности. Рынок сверхабсорбирующих полимеров — глобальный отраслевой анализ, размер, доля, рост, тенденции и прогноз, 2014-2020 гг. (2014).
- ↑ Alford DD, Wheeler AP, Pettigrew CA (1994). «Биодеградация термически синтезированного полиаспартата». J Environ Polym Degr . 2 (4): 225–236. DOI .
- Kelling K (2001). Реакция сельскохозяйственных культур на амисорб в Северо-Центральном регионе . Университет Висконсин-Мэдисон.
- К 2020 г. мировой рынок покрытий для бетонных полов будет стоить 1,1 млрд долларов США. Исследование рынка прозрачности (2015).
- Анализ рынка ингибиторов коррозии по продуктам, областям применения, отраслям конечного использования и прогнозы по сегментам до 2020 г. Grand View Research (2014)
- Salunkhe DK, Kadam S (18 августа 1995). . CRC Press. С. 368–. ISBN
- Considine DM (6 декабря 2012 г.). . Springer Science & Business Media. С. 114–. ISBN


































