Стереотаксическая радиохирургия на аппарате «Гамма-нож»
Стереотаксическая радиохирургия опухолей головного мозга – это подведение большой дозы излучения к мишени за одну фракцию (сеанс). Несмотря на свое название, стереотаксическая радиотерапия не является хирургической процедурой. Методика подразумевает высокоточную доставку к опухоли большой дозы ионизирующего излучения в обход рядом расположенных здоровых тканей.
Радиохирургическое лечение представляют собой важную альтернативу открытым хирургическим вмешательствам, особенно для пациентов, которые не в состоянии перенести операцию. Стереотаксическое облучение возможно также при опухолях, которые находятся рядом с жизненно важными отделами головного мозга или в труднодоступных для хирурга местах.
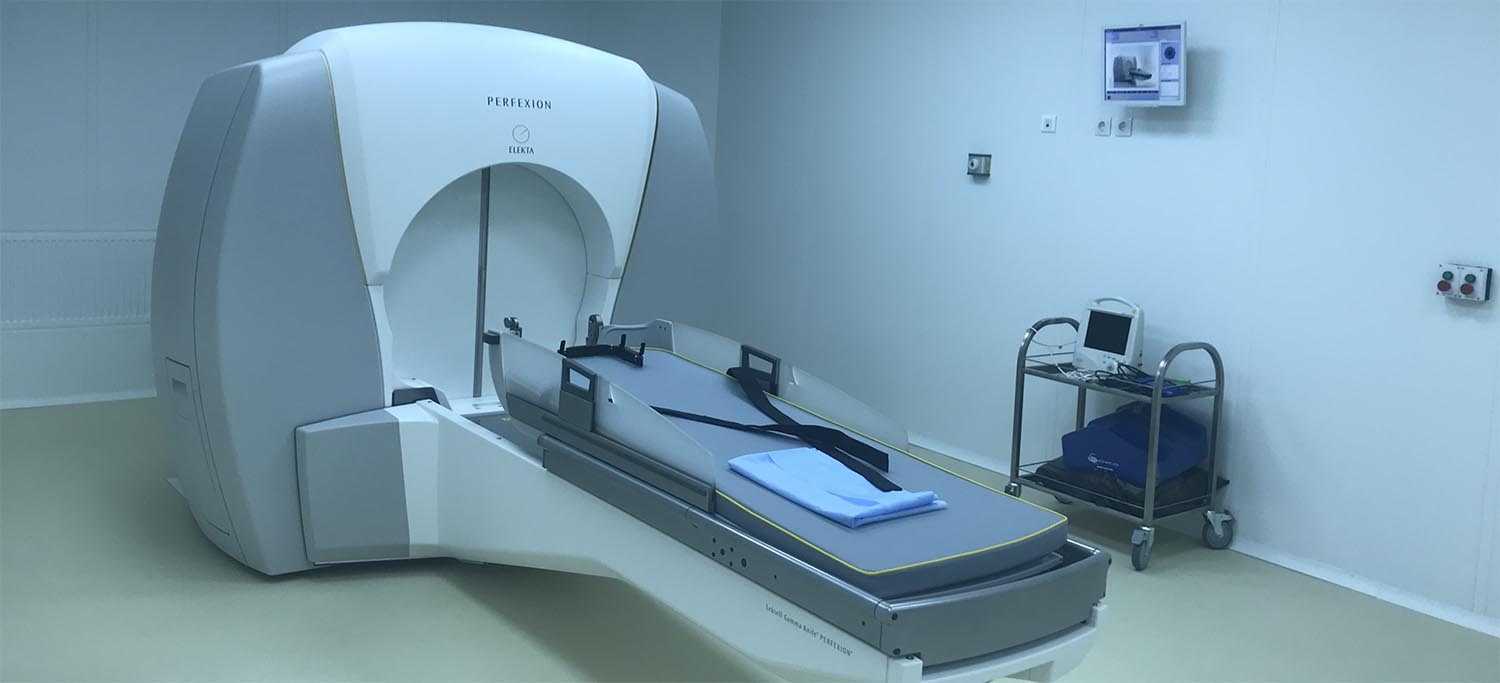
В настоящее время во всем мире насчитывается более 350 аппаратов «Гамма-нож», лечение по данной технологии получили, по некоторым оценкам, более 1 000 000 пациентов.
В РНПЦ ОМР им. Н.Н. Александрова радиохирургия проводится на самом современном радиотерапевтическом комплексе «Leksell Gamma Knife Perfexion» (Elekta), установленном в 2017 году.
Процедура выполняется под местной анестезией, возможно поведения лечения как в стационарных, так и в амбулаторных условиях в течение одного рабочего дня.
Сеанс радиохирургии состоит из 4 этапов:
- Фиксация навигационной рамы – осуществляется под местной анестезией и не сопровождается выраженными болевыми ощущениями.
- Выполнение навигационной магнитно-резонансной томографии (при необходимости – компьютерной томографии или прямой ангиографии).
- Планирование облучения.
- Сеанс радиохирургии на аппарате «Leksell Gamma Knife Perfexion» (Elekta), длительность которого может варьировать от десятков минут до нескольких часов в зависимости от сложности случая.
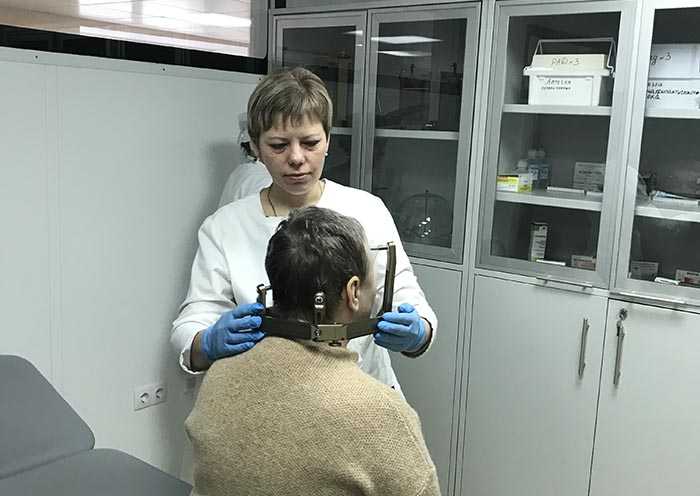
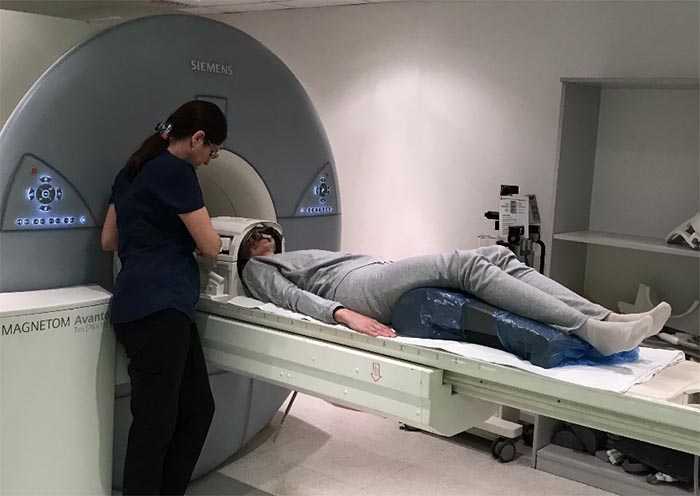
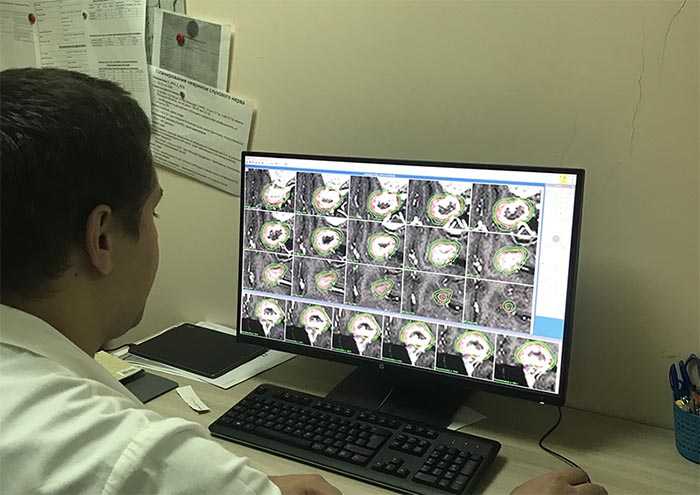
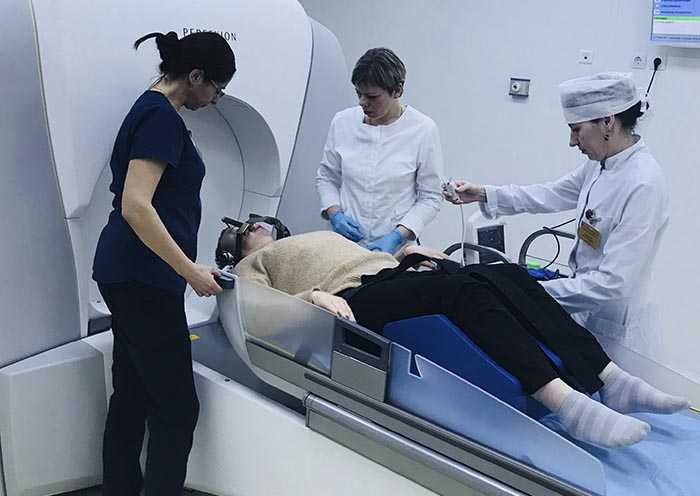
Процедура проводиться командой специалистов, в состав которой входят высококвалифицированные врачи-радиационные онкологи, рентгенологи и медицинские физики.
Показаниями к проведению радиохирургии на аппарате «Гамма-нож» являются:
- метастатическое поражение головного мозга (размер новообразования не более 3 см в наибольшем измерении, общее количество до 10, общее состояние пациента по шкале Карновского не менее 70%);
- невриномы черепно-мозговых нервов (не более 3 см в наибольшем измерении);
- менингиомы (не более 3 см в наибольшем измерении);
- аденомы гипофиза (не более 3 см в наибольшем измерении);
- артерио-венозные мальформации;
- краниофарингиомы;
- каверномы;
- пинеаломы;
- рецидивы злокачественных глиом головного мозга после проведенного ранее специального лечения (не более 3 см в наибольшем измерении).
Диагностические мероприятия
Вначале обследование проводит детский врач-гастроэнтеролог, который изучает семейный анамнез, измеряет температуру тела маленького пациента, знакомится с историей его болезни, собирает и анализирует жизненный анамнез, пальпирует переднюю стенку полости брюшины, опрашивает родителей, когда проявились признаки заболевания.
Далее назначаются лабораторные и инструментальные диагностические методы.
Лабораторные методы диагностики:
- Анализы крови (общий, биохимический);
- Выявление онкомаркеров;
- Пробы печени;
- Лабораторный анализ биоптата.
Инструментальными методами диагностики называют:
- Рентгенографию;
- КТ;
- МРТ;
- Ангиографию;
- Ультрасонографию;
- Радиоизотопное сканирование;
- Биопсию.
Важную роль в постановке диагноза играет различительная диагностика, в ходе которой необходимо различить гепатобластому и иные заболевания, например, псевдокисту либо патологию Вильмса.
Постановка точного диагноза позволяет составить эффективную лечебную тактику.
Медицинское наблюдение после операции
После операции по удалению желчного пузыря врач-хирург зачастую не дает никаких долгосрочных рекомендаций. Однако чтобы избежать повторных операций, осложнений и возобновления симптомов желчнокаменной болезни, необходимо:
- 1-2 раза в год — посещение гастроэнтеролога для оценки состояния гепатобилиарной зоны
- 1-2 раза в год — УЗИ органов брюшной полости, в частности УЗИ холедоха (общего желчного протока)
- постоянный или курсовой прием препаратов для разжижения желчи (урсодезоксихолиевая кислота — УДХК) и спазмолитиков согласно рекомендациям лечащего врача-гастроэнтеролога.
Как проходит лапароскопическая простатэктомия?
Вне зависимости от выбранной технологии, удаление предстательной железы займет около 3 часов. За это время хирург последовательно выполнит несколько этапов простатэктомии:
Анестезия
Операция проводится под эндотрахеальным наркозом или комбинированной анестезией. Пациент полностью погружается в сон и не чувствует боли и дискомфорта.
 Анестезия
Анестезия
Доступ к предстательной железе
На этом этапе врач делает несколько проколов в брюшной стенке или, введя инструменты в кишечник, прокалывает заднюю часть мочевого пузыря. При этом вместе с хирургическими инструментами в зону проведения операции вводится видеокамера и осветительное оборудование.
Непосредственно удаление простаты
Добравшись до простаты, врач аккуратно удаляет орган, семенные пузырьки и окружающие железу лимфатические узлы. Каждое движение хирург видит на экране компьютера, что позволяет минимально травмировать ткани и сосудистые стенки.
Создание анастомоза
После удаления простаты между уретрой и мочевым пузырем образуется свободное пространство. Эти органы объединяют, создавая анастомоз (соединение). В эту область врач устанавливает катетер — для выведения из организма жидкости.
Окончание операции
Хирург извлекает инструменты. Удаленные ткани направляет на гистологический анализ для выявления раковых клеток. При необходимости пациенту накладывают швы.
Лапароскопическая простатэктомия — сложная операция, требующая навыков и знаний врача. Особенно тяжело приходится хирургу при работе с пациентами, у которых узкий таз, ведь пространство для действий в этом случае ограничено.
Профилактика геморрагического инсульта и повторного приступа
После перенесённого инсульта больные долго находятся под врачебным наблюдением. У них проверяется уровень сахара и другие кровяные показатели, контролируется АД. Это помогает избежать повторного удара, который, как правило, стоит больному жизни.
Чтобы не допустить повторного инсульта, нужно:
- Аккуратно выполнять врачебные рекомендации и принимать назначенные лекарства.
- Сбалансировать питание, исключив жирное, жареное, конченое, фосфид и трудноусвояемую еду.
- Делать упражнения, утреннюю гимнастику, больше ходить. Это помогает разрабатывать конечности и насыщать организм кислородом.
- Отказаться от вредных привычек и зависимостей.
- Стараться меньше нервничать.
Более 50% кровоизлияний в мозг обусловлены повышением АД, поэтому люди, страдающие гипертонией, находятся в группе риска. Чтобы избежать возникновения инсультов, им нужно поддерживать давление на нормальном уровне, принимая антигипотензивные средства. Особенно опасно сочетание гипертонии и диабета. Сосуды, потерявшие прочность и эластичность из-за сахарной болезни, разрываются чаще, поэтому больным нужно следить на АД и уровнем глюкозы в крови.
Вторая причина возникновения кровоизлияний – травмы головы. При слабовыраженном повреждении сосудов инсульт может развиться не сразу. Поэтому при любом травматическом поражении головы нужно обязательно показаться врачу, чтобы исключить кровоизлияние.
Часто разрыв сосудов возникает из-за врожденных дефектов (аневризм, мальформаций). Больные долгое время страдают от головных болей и даже эпилептиформных припадков, не обследуясь должным образом. В результате они погибают от разрыва сосуда и массивного излития крови в головной мозг. Такой инсульт возникает у молодежи и даже у детей. Он стоил жизни 20-летнему подающему надежды шахматисту Ивану Букавшину и тренеру ЦСКА 45-летнему Сергею Шустикову. Если бы эти люди тщательно обследовались, их бы можно было спасти, проведя плановую операцию.
Вызывает инсульт длительный прием препаратов, влияющих на свертываемость крови. Если врач прописал такие лекарства, нужно постоянно сдавать анализы крови и не превышать рекомендованных сроков и доз.
Немаловажную роль в возникновении геморрагических инсультов играют вредные привычки. Болезнь чаще возникает у курильщиков и у людей, склонных к употреблению спиртного и наркотиков. Особенно часто инсульт возникает у людей с опиатной зависимостью.
Правосторонняя гемигепатэктомия
Требует рассечения печеночно-почечной, правой треугольной, печеночно-диафрагмальной и серповидной связок. Правые ветви воротной вены, печеночной артерии и правый печеночный проток перевязывают.
Как только завершился воротный этап оперативного вмешательства, правая верхняя, срединная и нижняя вены, а также мелкие печеночные, правые притоки срединной печеночной вены также перевязываются хирургом.
В ходе операции после удаления доли печени обеспечивают дополнительный гемостаз и холестаз по линии иссечения. Для того, чтобы обнаружить маленькие по диаметру желчные протоки, в печеночный проток вводят раствор метиленового синего.
Культю органа укрывают большим сальником. Заключительный этап операции – декомпрессия печеночного протока через общий желчный или пузырный проток в зависимости от предыдущих поэтапных действий. Дренажи устанавливают в правую область плевры и в культю печени.
Период восстановления
После хирургического вмешательства пациент должен в течение 7 суток находиться на дневном стационаре. Это период восстановления организма. Если имеются послеоперационные осложнения, срок продлевают.
В дневном стационаре за пациентом ухаживают, оказывая следующие услуги:
- в первые несколько суток пациент получает питание через капельницу;
- ежедневно меняется повязка, наложенная на область раны;
- пациент должен употреблять болеутоляющие препараты и лекарственные вещества, позволяющие бороться с тошнотой;
- помощь в выполнении личной гигиены после оперативного вмешательства.
Показания
К основным показаниям для резекции относят:
- травмы печени;
- первичные злокачественные новообразования органа;
- множественные абсцессы;
- альвеолярный эхинококк;
- поликистоз;
- злокачественные образования на других органах, например, на толстой кишке.
Если патологический процесс распространен, требуется иссечение более половины органа. Такое оперативное вмешательство называется расширенной гемигепатэктомией. При правосторонней операции резецируют правую анатомическую долю органа и четвертый сегмент левой половины.
Расширенная левосторонняя гемигепатэктомия выполняется в двух вариантах:
- полное иссечение левой половины и правого около срединного сектора;
- резекция левой доли печени и пятого сегмента правой стороны.
Перед проведением операции требуется точно установить топический и нозологический диагнозы. Для этого проводят трансумбиликальную гепатопортографию и спленопортографию.
Подход к реабилитации в «Парамита»
 Прием пациента в период реабилитации в нашей клинике
Прием пациента в период реабилитации в нашей клинике
В московской клинике «Парамита» реабилитация после операции по удалению грыжи позвоночника проходит поэтапно. Подробная программа восстановления устанавливается, исходя из:
- истории болезней;
- сложности операций;
- сопутствующих болезней;
- возраста;
- пола;
- физических возможностей;
- данных лабораторных анализов, рентгена, МРТ и т.д.
Наши врачи с каждым больным после удаления грыжи работают по индивидуальной программе. В лечении грыжи мы используем как западные, так и восточные методы – физиотерапию, массаж, гирудотерапия, иглоукалывание и др.
В распоряжении центра – современное оборудование, которое помогает быстро восстановиться после операции. Врачи внимательно следят за ходом реабилитации, вовремя корректируют программу. Мы всегда на связи с нашими пациентами, мгновенно отвечаем на все обращения.
Техника операции
Обезболивание — эндотрахеальный наркоз с управляемым дыханием.
Хирургический доступ при Гемигепатэктомии должен обеспечивать возможность хорошего подхода к воротам печени, нижней полой и печеночным венам. Для левосторонней Г. обычно используют абдоминальные доступы: верхнюю срединную лапаротомию (при необходимости дополненную срединной стернотомией) или комбинированный разрез Брегадзе — параллельно левой реберной дуге с переходом на VIII межреберье справа. Правосторонняя Г. выполняется из торако-френо-абдоминального доступа. В зависимости от высоты стояния правого купола диафрагмы торакотомия (см.) производится по VI, VII или VIII межреберьям, а лапаротомия (см.) — от реберной дуги к пупку. Целесообразно произвести сначала абдоминальную часть разреза и из него осуществить ревизию брюшной полости. В случае операбельности разрез расширяют на грудную стенку.
Существуют три методики обработки сосудов печени при Г.: 1) перевязка в воротах без предварительного рассечения печени; 2) перевязка по мере их обнаружения, с подходом к ним через паренхиму печени в относительно бессосудистых участках (по линии Рекса — Кантли) — так наз. фиссуральный способ; при фиссуральном доступе к сосудам ножка печени временно пережимается; 3) промежуточная техника, объединяющая в себе элементы первых двух.
Хирурги в странах Европы, Америки и в СССР чаще применяют перевязку сосудов и желчных протоков в воротах печени и реже фиссуральный способ.
Хирурги некоторых стран Азии, имеющие наибольший опыт Г.,— Тон Тхат Тунг, Накаяма, Лин (K.Nakayama, Т. Lin) пользуются почти исключительно фиссуральным способом. К преимуществам этого метода они относят ускорение операции, меньшую кровопотери) и возможность безопасной обработки сосудов при многочисленных вариантах их ветвления в воротах. Лин (1960) опубликовал метод операции, заключающийся в пальцевом разделении паренхимы и контроле встречных сосудов. Накаяма (1958) пользуется специальным зажимом, который разрывает паренхиму печени, но задерживается на сосудах.
Правосторонняя гемигепатэктомия
Для мобилизации правой половины печени рассекают правую треугольную, серповидную, печеночно-диафрагмальную и печеночно-почечную связки. Тупо отпрепаровывают внебрюшинное поле печени от диафрагмы. В воротах печени перевязывают правые ветви воротной вены и печеночной артерии, затем правый печеночный проток. Правую ветвь печеночной артерии до перевязки временно пережимают и убеждаются, что она не снабжает левую половину печени.
После окончания воротного этапа операции перевязывают правую верхнюю, правую среднюю и нижнюю вены, правые притоки средней печеночной вены и отдельные мелкие печеночные вены.
После удаления правой доли осуществляют дополнительный гемостаз и холестаз по линии сечения. Для обнаружения мелких желчных протоков вводят р-р метиленового синего в печеночный или общий желчный проток.
Культю печени укрывают большим сальником, связками или лоскутом диафрагмы. Операцию завершают декомпрессией печеночного протока через культю пузырного (если производилась холецистэктомия) или через общий желчный проток по Керу, Вишневскому или Дольотти (см. Желчные протоки, операции). Резиновые дренажи подводят к культе печени и в правую плевральную полость.
Что лучше: стент или шунт?
Если сравнить две методики коррекции ишемии и гипоксии миокарда через питающие мышцу сосуды, то становятся очевидными достоинства и недостатки стентирования и шунтирования сосудов сердца:
| Оценочный критерий | Стентирование | Шунтирование |
|---|---|---|
| Объем вмешательства | Минимальный, внутрисосудистый | Технически сложное вмешательство |
| Длительность операции | От часа до трех | От трех до девяти и более |
| Остановка сердца | Не нужна | Более половины операций проходят с остановленным сердцем |
| Разрез | Исключен | Рассекается грудина |
| Обезболивание | Местное, реже – с учетом индивидуального порога болевой чувствительности | Глубокий наркоз |
| Реабилитация | Несколько дней | До полугода |
| Острые случаи | Практикуется купирование ОИМ | Не допускается из-за тяжести вмешательства |
| Капилляры | Возможна коррекция сосудов с диаметром от 3мм | Невозможно корректировать мелкие ветви |
| Реставрация кровотока | На несколько лет | До 10 лет и более |
Общие принципы операций на печени
Негласным правилом в гепатологии считается, что удаление более 70% тканей органа при здоровой или более 60% при нарушенной печеночной функции приводит к тяжелым послеоперационным осложнениям. Это связано с неспособностью оставшейся части печени справиться со своими метаболическими обязанностями.
Технические проблемы при вмешательствах на печени обусловлены несколькими факторами:
- сложность создания полноценного оперативного доступа к органу;
- богатое кровоснабжение печени, приводящее к повышенному риску массивного кровотечения;
- большое количество трубчатых структур (сосуды, желчные пути), требующих перевязки перед пересечением;
- мягкая консистенция органа обуславливает сложность его ушивания.
Для нивелирования перечисленных сложностей используется ряд оперативных приемов и техник. Во-первых, при хирургических вмешательствах на печени используется специальный инструментарий: реберные ретракторы, электрокоагуляторы с дополнительными насадками и ножи, ультразвуковые деструкторы-аспираторы, сосудистые зажимы для печеночных вен, клипаторы для сосудов и желчных протоков, аппараты для реинфузии (обратное вливание) крови, гемостатические пленки и губки.
Во-вторых, для обеспечения хорошего поля деятельности прибегают к специальным хирургическим доступам. Они предполагают большие разрезы, проходящие как по правой половине грудной клетки, так и по передней брюшной стенке. Существует более 70 модификаций доступов к печени (по Куино, Петровского-Почечуеву, Боровскому и другие). Большинство из них являются травматичными, а некоторые предполагают и резекцию участков ребер.
Выбор доступа осуществляется индивидуально, исходя из объема планируемой резекции. Однако общепризнанным и самым удобным признается двухподреберный доступ с вертикальным продолжением. Он предполагает разрезы под реберными дугами и по срединной линии живота. Мечевидный отросток грудины при этом удаляется. Основные преимущества этого доступа — удобство работы при любом типе операции и широкое рабочее поле для хирургов.
В-третьих, оперативная техника на печени предполагает использование специальных приемов. Например, для ушивания раны используются специальные гемостатические швы. Их выполняют тупоконечной атравматической иглой и нитью. Для быстрого и прочного ушивания наглухо сосудов или желчных путей также могут применяться клипаторы. В ходе хирургического вмешательства также нередко прибегают к интраоперационному УЗ-исследованию печени и другим инвазивным методам исследования.
Список использованной литературы:
- Ангиография и чрескатетерные эндоваскулярные вмешательства при кровотечениях из варикозно расширенных вен пищевода. Всесоюзная конференция «Лучевая диагностика и рентгенодиапевтика заболеваний печени и почек», Ленинград, 1984, стр. 22-24 (соавт. В.И.Прокубовский, М.Н.Овчининский, С.А.Капранов).
- Возможности и перспективы развития рентгено-эндоваскулярных вмешательств при кровотечениях из варикозно расширенных вен пищевода. VII Всесоюзный симпозиум «Рентгеноэндоваскулярная хирургия», 1985, стр. 133-134 (соавт. М.Н.Овчининский, В.А.Черкасов, С.А.Капранов, С.Б.Бахвалов).
- Методика и тактика эндоваскулярного гемостаза при профузных кровотечениях из варикозно расширенных вен пищевода. Республиканская конференция хирургов «Хирургическое лечение портальной гипертензии, заболеваний и травм печени», Харьков, 1986, стр. 60-62 (соавт. В.И.Прокубовский, М.Н.Овчининский, В.А.Черкасов, С.А.Капранов).
- Пути повышения эффективности эндоваскулярных вмешательств при кровотечениях из варикозно расширенных вен пищевода. Республиканская научно-практическая конференция «Рентгено-контрастные методы исследования и эндоваскулярная хирургия», Алма-Ата, 1986, стр. 167-169 (соавт. В.А.Черкасов, М.Н.Овчининский, С.А.Капранов).
- Способ комплексной эмболизации варикозно расширенных вен пищевода и желудка. Рационализаторское предложение отраслевого значения 0-2976 от 2.10.1987 (соавт. М.Н.Овчининский, С.А.Капранов, А.С.Беленький).
История метода минифлебэктомии (микрофлебэктомии) вен
Основателем методики минифлебэктомии вен принято считать Роберта Мюллера, швейцарского дерматолога, флеболога. Впервые доктор Мюллер применил метод минифлебэктомии в 1950-х годах, так как доктор не был удовлетворён результатами как склерооблитерации, так и хирургического удаления отдельных венозных сосудов. Роберту Мюллеру хотелось получить альтернативную методику радикального удаления вен, но без побочного эффекта в виде крупных, бросающихся в глаза, шрамов после классических операций. Метод минифлебэктомии был представлен швейцарским доктором на ежегодном собрании Французского общества флебологов в 60-х годах прошлого столетия после примерно 10-летнего самостоятельного практического применения. В последующие годы технология усовершенствовалась и развивалась, появились новые приёмы манипуляций, более современные инструменты (крючки).

Профессор Золтан Варади
Наибольший вклад в этот процесс внёс Золтан Варади, серьёзно модифицировав методику и придав ей новые векторы развития.
Осложнения
Часто после оперативного вмешательства у пациента возникает чувство боли, жара, дискомфорта за грудиной. Это не повод для паники, нужно сообщить об этом врачу, который назначит купирующие препараты. Самые частые осложнения после шунтирования сосудов сердца: застой в легких, анемия, перикардит и другие воспалительные процессы, флебит близлежащих к шунту вен, иммунные нарушения (при остановке сердца), аритмии.
Для предупреждения застойных явлений в легких рекомендуется до 20 раз/день надувать воздушные шарики. Анемия купируется специальной диетой, при необходимости – гемотрансфузиями. Лечение других осложнений индивидуально для каждого пациента.
Минифлебэктомия или микросклерозирование?
Минифлебэктомия — операция, во время которой пораженную вену удаляют без разрезов кожного покрова через небольшие проколы. Она может быть самостоятельной операцией, но чаще комбинируется с прочими методами терапии варикозной болезни.
Как самостоятельный метод лечения минифлебэктомия применяется в таких случаях:
- на начальных стадиях варикозной болезни;
- при удалении притоков большой/малой подкожной вены (при условии отсутствия рефлюкса по основному стволу);
- при ограниченных варикозных узлах;
- при расширенных венах на нетипичных участках тела;
- для удаления вены после проведенного основного лечения тромбофлебита;
- при восходящем тромбофлебите подкожной вены.
Минифлебэктомия в качестве дополнительной операции может сочетаться:
- с перевязкой перфорантных вен;
- эндовазальной лазерной коагуляцией;
- удалением притоков после кроссэктомии основного ствола подкожной вены.
Минифлебэктомия обладает хорошим косметическим эффектом, не имеет возрастных ограничений и исключает необходимость в повторных процедурах, поскольку отсутствует риск рецидива.
Микросклеротерапия — щадящая методика, применимая на ранних этапах развития варикоза. Она показана для удаления расширенных подкожных капилляров. С ее помощью можно убрать варикозные сеточки и змееподобно расширенные вены.
В полость сосуда вводится склерозант, который в буквальном смысле склеивает его стенки. Минусом этого метода, в отличие от минифлебэктомии, является высокая вероятность рецидива варикозной болезни. Однако этого можно избежать, если следовать профилактическим рекомендациям: правильно питаться, исключить чрезмерные физические нагрузки, избавиться от лишнего веса.
Послеоперационный период
Восстановление обычно занимает 3–4 недели, первая из которых проходит в стационаре. Это необходимо чтобы вовремя отреагировать на самое частое осложнение тонзиллэктомии – глоточного кровотечения. Для его предупреждения назначают кровоостанавливающие препараты.
Из операционной пациента переводят в палату под наблюдение лечащего врача. В первые сутки запрещено глотать, сплевывать или отхаркивать слюну. Дышать можно только через рот. При выраженном болевом синдроме пациенту назначают обезболивающие препараты.
Все дни послеоперационного периода рекомендована диета
- в первые сутки взрослым следует воздерживаться от приема пищи, а маленьким детям нельзя есть или пить в ближайшие 6 часов;
- в первую неделю после операции рекомендуется есть жидкую однородную пищу;
- на протяжении восстановительного периода пища должна быть мягкой, не рекомендуется есть слишком горячее, холодное, кислое, острое. Это может раздражать слизистую горла и ротовой полости.
- В послеоперационном периоде при необходимости назначают курс антибиотиков.
Постельный режим нужно соблюдать в течение 2 дней. В большинстве случаев пациента выписывают из стационара в течение недели на амбулаторное наблюдение и лечение.
Подготовка к процедуре
Алгоритм подготовительного этапа по замене дренажа при послеоперационной перевязке включает:
- Гигиеническое очищение рук медперсоналом.
- Использование перчаток во время выполнения процедуры.
- Идентификацию пациента.
- Представление, объяснение больному задачи и последовательности предстоящей манипуляции.
- Получение добровольного согласия пациента на процедуру.
- Получение от пациента информации относительно того, приносит ли ему дренаж какой-либо дискомфорт (в том случае, когда больной находится в сознании).
- Повторная гигиеническая обработка рук антисептиком, их осушение.
- Подготовка всех необходимых для манипуляции средств.
- Подготовка ёмкости с дистиллированной водой или физиологическим раствором.
- Подготовка дренажной системы (трубки для отведения гнойного содержимого должны быть стерильны и правильно подобраны по размеру).
- Замена старого дренажа новым.
- Закрытие раны чистой стерильной повязкой.
Симптоматические проявления
Симптоматические проявления заболевания, как правило, не носят ярко выраженного характера. Проблема осложняется и тем, что большинство заболевших – дети, которые не могут объяснить, в чем причина их беспокойства.
Среди симптоматических проявлений патологии клиническая практика указывает на:
- Бледность кожи и ее желтый оттенок;
- Заметно увеличенную полость брюшины;
- Уплотнение в зоне локализации печени;
- Высокую температуру;
- Подавленность;
- Слабость;
- Болезненность;
- Резкую потерю веса;
- Потерю аппетита;
- Повышенную плаксивость;
- Осветление кала;
- Потемневшую мочу;
- Желтушность склер глаз и слизистых оболочек.
Гипернефрома
Все перечисленные симптомы могут указывать на быстроразвивающуюся опухоль, которая, по мере своего роста, распространяется на другие органы и поражает их. Поражение может коснуться:
- Брюшины;
- Легких;
- Костной системы;
- Головного мозга.
При поражении перечисленных органов основные симптомы заболевания могут быть дополнены иными характерными симптоматическими проявлениями.

































